

2022 , Vol. 16 >Issue 05: 315 - 318
DOI: https://doi.org/10.3877/cma.j.issn.1674-0807.2022.05.009
腋窝单孔腔镜辅助下乳房切除术加一期乳房重建研究进展
收稿日期: 2020-05-22
网络出版日期: 2022-11-10
版权
Axillary single-port endoscopic mastectomy plus stage I breast reconstruction
Received date: 2020-05-22
Online published: 2022-11-10
Copyright
李芸 , 明佳 . 腋窝单孔腔镜辅助下乳房切除术加一期乳房重建研究进展[J]. 中华乳腺病杂志(电子版), 2022 , 16(05) : 315 -318 . DOI: 10.3877/cma.j.issn.1674-0807.2022.05.009
表1 腋窝单孔腔镜辅助下乳房切除术加一期乳房重建的临床研究 |
| 临床研究 | 例数 | 年龄(岁) | 肿瘤大小(cm) | 临床分期(例) | |||||
|---|---|---|---|---|---|---|---|---|---|
平均(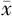 ±s) ±s) | 范围 | 平均(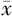 ±s) ±s) | 范围 | 0期 | Ⅰ期 | Ⅱ期 | Ⅲ期 | ||
| Lai等[4] | 11 | 50.9±7.3 | 37.9~66.9 | 3.41±2.33 | 0.4~6.9 | 4 | 3 | 2 | 2 |
| 姚天琦等[6] | 10 | NA | 32~53 | NA | 1.0~2.9 | 6 | 4 | 0 | 0 |
| Lai等[7] | 21 | 48.9±11.6 | NA | 2.8±1.2 | NA | 4 | 7 | 8 | 2 |
| 黄贞强等[8] | 15 | 37.5b | 27~45 | 2.6±0.3 | 1.5~3.0 | 0 | 5 | 10 | 0 |
| 王子函等[9] | 12 | 45.5±8.7 | 32~58 | 1.98±0.89 | 1.0~3.5 | 4 | 8 | 0 | 0 |
| Toesca等[10] | 24a | 42b | 30~55 | 1.7±0.4 | 0~3.2 | 5 | 7 | 2 | 0 |
| Tukenmez等[12] | 10 | 41±7 | 30~51 | 1.41±0.65 | 0.8~2.9 | 2 | 6 | 2 | 0 |
| 关山等[14] | 21 | 44±9 | 33~60 | NA | ≤5 | 4 | 17 | 0 | 0 |
| Wan等[15] | 30 | 44.57±8.84 | NA | NA | NA | 5 | 4 | 17 | 4 |
| Lai等[16] | 50 | 45.3±8.4 | 31~62 | 浸润性癌为2.3±1.8;原位癌为2.6±1.7 | 浸润性癌为0.1~7.3;原位癌为0.2~5.7 | 15 | 10 | 14 | 11 |
| 临床研究 | 例数 | 手术时间(min,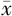 ±s) ±s) | 术中出血量(ml,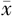 ±s) ±s) | 随访时间(月,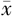 ±s) ±s) | 局部复发(例) | 远处转移(例) | 满意度 | 住院时间(d) | |
| Lai等[4] | 11 | 181.8±32.4 | 38.3±45.3 | NA | 0 | 0 | 93.3 | NA | |
| 姚天琦等[6] | 10 | 250±61 | 45.4±3.9 | 3b | 0 | 0 | 100 | 5 | |
| Lai等[7] | 21 | 279.8±79.3 | 37.0±38.2 | 6.9±3.5 | 0 | 0 | 100 | NA | |
| 黄贞强等[8] | 15 | NA | NA | 11b | 0 | 0 | 93.3 | NA | |
| 王子函等[9] | 12 | 280.8±78.5 | 32.0±20.2 | 5.5±1.9 | 0 | 0 | 100 | NA | |
| Toesca等[10] | 24 | NA | NA | 8b | 0 | 0 | NA | 2 | |
| Tukenmez等[12] | 10 | 250b | NA | 3b | 0 | 0 | 100 | 3 | |
| 关山等[14] | 21 | 185±43 | 60±48 | NA | 0 | 0 | 76.2 | NA | |
| Wan等[15] | 30 | 180b | NA | 27.77±20.43 | 0 | 1 | 96.67 | NA | |
| Lai等[16] | 50 | 244.3±82.8 | 74.5±47.7 | 21.6±11.3 | 0 | 0 | 94.4 | NA | |
注:a24例患者中5例乳房为预防性切除,无肿瘤分期;b为中位值;NA指文献未提及 |
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
姚天琦,朱正才,李涛,等.单孔腔镜下保留乳头乳晕复合体乳房切除术中即刻乳房重建的效果[J]. 江苏医药,2019,45(12),1280-1282.
|
| [7] |
|
| [8] |
黄贞强,陈凯,朱李玲,等.经腋窝切口腔镜下乳房皮下腺体切除联合即刻乳房重建的疗效观察[J]. 中国修复重建外科杂志,2018, 32(11):99-103.
|
| [9] |
王子函,张玉龙,王捷,等.保留乳头乳晕的单孔法腔镜皮下乳腺切除术治疗早期乳腺癌的临床疗效[J]. 腹腔镜外科杂志,2018,23(3):34-39.
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
关山,王宇,张开通,等.应用皮肤悬吊系统腔镜下保留乳头乳晕乳腺切除即刻乳房重建[J].中华外科杂志,2017,55(2):126-129.
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
陈涛,贾琳娇,翟保平,等. 腔镜辅助乳房重建手术方式的研究进展[J/CD]. 中华乳腺病杂志(电子版), 2019, 13(2):66-68.
|
| [25] |
|
| [26] |
洪小芳,刘晓韬,孟宏,等.游离腹壁下动脉穿支皮瓣在乳房再造中的应用[J].中国美容医学,2014,23(19):1595-1597.
|
| [27] |
万能斌,刘德权,卢伶俐,等.带蒂大网膜瓣在乳腺癌术后乳房再造中的应用研究[J].中国修复重建外科杂志,2019(8):1006-1010.
|
| [28] |
|
/
| 〈 |
|
〉 |