

2021 , Vol. 15 >Issue 06: 346 - 351
DOI: https://doi.org/10.3877/cma.j.issn.1674-0807.2021.06.003
乳腺癌新辅助化疗后雌、孕激素受体表达变化的临床意义
收稿日期: 2020-08-11
网络出版日期: 2022-02-07
版权
Clinical significance of estrogen receptor/progesterone receptor expression changes in breast cancer patients after neoadjuvant chemotherapy
Received date: 2020-08-11
Online published: 2022-02-07
Copyright
探讨乳腺癌患者新辅助化疗(NAC)前后ER、PR表达变化与NAC疗效之间的关系。
回顾性分析从2015年1月到2017年6月在解放军总医院第五医学中心行蒽环类联合紫杉类NAC后肿瘤未达到pCR的127例HER-2阴性浸润性乳腺癌患者的临床资料。通过免疫组织化学方法测定NAC前后肿瘤组织中ER、PR的表达。分别按照核染色比例≥1%、>10%和>20%来定义ER、PR阳性,判断NAC前后ER和PR的表达状态,两者完全一致为一致组,否则为差异组。用χ2检验或秩和检验比较一致组和差异组的临床病理特征,t检验或秩和检验比较2组的肿瘤缓解率。进一步分析差异组中ER、PR的变化状态,分为ER阴转阳、ER阳转阴、PR阴转阳和PR阳转阴4个亚组,采用方差分析对3种标准下4个亚组的肿瘤缓解率进行比较。
以1%为界值,一致组与差异组患者的临床病理特征比较,差异无统计学意义(P均>0.050)。以10%为界值,2组在PR表达上差异有统计学意义(χ2=4.757,P=0.029)。以20%为界值,差异组中腋窝淋巴结转移、ER、PR阳性及三阴性乳腺癌的比例更高(χ2=5.572、8.683、11.724、4.686,P=0.018、0.003、0.001、0.030)。以1%为界值,一致组和差异组的肿瘤缓解率分别为(35.9±26.8)%、(46.8±23.8)%,差异有统计学意义(t=2.190, P=0.032)。以10%及20%为界值,一致组和差异组的肿瘤缓解率比较,差异无统计学意义[M(P25,P75):37.3(21.4,53.6)%比38.5(26.8,54.7)%, Z=0.446, P=0.656; 39.1(22.7,55.1)%比39.5(27.3, 56.9)%, Z=0.548, P=0.584]。在核染色比例≥1%、>10%和>20% 3种标准下,4个亚组肿瘤缓解率比较,差异均无统计学意义(F=1.380、1.890、1.970,P=0.266、0.146、0.131)。
当ER、PR以核染色比例≥1%为阳性标准时,NAC后ER或者PR状态变化的乳腺癌患者有望获得更高的肿瘤缓解率。NAC后ER、PR状态的不同变化并不会对NAC的疗效产生影响。
陈圣 , 朱明华 , 黄焰 , 王怀涛 , 何奇 . 乳腺癌新辅助化疗后雌、孕激素受体表达变化的临床意义[J]. 中华乳腺病杂志(电子版), 2021 , 15(06) : 346 -351 . DOI: 10.3877/cma.j.issn.1674-0807.2021.06.003
To explore the relationship between the expression changes of estrogen receptor (ER)/progesterone receptor (PR) before and after neoadjuvant chemotherapy (NAC) and the efficacy of NAC in breast cancer patients.
The clinical data of 127 patients with HER-2-negative invasive breast cancer who had not achieved pCR after NAC (anthracycline and docetaxel-based regimen) in the Department of Pathology, Fifth Medical Center, General Hospital of PLA from January 2015 to June 2017 were retrospectively analyzed. ER and PR expressions in tumor tissues before and after NAC were determined by immunohistochemistry. ER/PR was regarded as positive if nuclear staining percentage ≥1%, > 10% or > 20%, respectively. The patients with different ER/PR expression status before and after NAC were in Group A, and others were in Group B. The χ2 test or rank sum test was used to compare the clinicopathological characteristics between two groups. The t test or rank sum test was used to compare the tumor remission rates between two groups. According to the different change of ER and PR after NAC, Group A was divided into 4 subgroups: ER negative to positive subgroup, ER positive to negative subgroup, PR negative to positive subgroup and PR positive to negative subgroup. Analysis of variance was used to compare the tumor remission rates among 4 subgroups under the three positive expression standards.
With nuclear staining percentage ≥1% as the positive standard, there was no statistically significant difference in clinicopathological characteristics between two groups (all P>0.050). With nuclear staining percentage >10% as the positive standard, PR expression showed a significant difference between two groups (χ2=4.757, P=0.029). With nuclear staining percentage >20% as the positive standard, Group A had higher rates of axillary lymph node metastasis, ER positive, PR positive and triple negative breast cancer compared with Group B (χ2=5.572, 8.683, 11.724, 4.686; P=0.018, 0.003, 0.001, 0.030). With nuclear staining percentage ≥1% as the positive standard, the tumor remission rate was (46.8±23.8)% in Group A, (35.9±26.8)% in Group B, indicating a significant difference (t=2.190, P=0.032). With nuclear staining percentage >10% or >20% as the positive standard, the tumor remission rate showed no significant difference between Group A and Group B[M(P25, P75): 38.5(26.8, 54.7)% vs 37.3(21.4, 53.6)%, Z=0.446, P=0.656; 39.5(27.3, 56.9)% vs 39.1(22.7, 55.1)%, Z=0.548, P=0.584]. Under the three positive expression standards (≥1%, >10% and >20%), there was no significant difference in tumor remission rate among four subgroups (F=1.380, 1.890, 1.970; P=0.266, 0.146, 0.131).
With nuclear staining percentage≥10% as the positive standard, the change of ER/PR status after NAC may indicate a higher tumor remission rate. The different changes of ER/PR status after NAC have no impact on the efficacy of NAC.
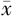 ±s表示,用 t检验比较;以10%及20%为界值,2组肿瘤缓解率数据经检验不符合正态分布,用M(P25,P75)表示,采用秩和检验进行比较。各个亚组的肿瘤缓解率均符合正态分布,用
±s表示,用 t检验比较;以10%及20%为界值,2组肿瘤缓解率数据经检验不符合正态分布,用M(P25,P75)表示,采用秩和检验进行比较。各个亚组的肿瘤缓解率均符合正态分布,用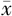 ±s表示,组间比较采用方差分析。所有的统计分析进行双侧检验,检验水准α=0.050。
±s表示,组间比较采用方差分析。所有的统计分析进行双侧检验,检验水准α=0.050。表1 在不同阳性判定标准下新辅助化疗前后ER、PR表达一致组与差异组乳腺癌患者的临床特征比较 |
| 临床病理特征 | ≥1% | >10% | >20% | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 一致组(n=91) | 差异组(n=36) | 检验值 | P值 | 一致组(n=86) | 差异组(n=41) | 检验值 | P值 | 一致组(n=80) | 差异组(n=47) | 检验值 | P值 | ||
| 年龄 | |||||||||||||
| ≤50岁 | 56 | 26 | χ2=1.287 | 0.257 | 54 | 28 | χ2=0.367 | 0.544 | 53 | 29 | χ2=0.268 | 0.605 | |
| >50岁 | 35 | 10 | 32 | 13 | 27 | 18 | |||||||
| 绝经 | |||||||||||||
| 是 | 31 | 12 | χ2=0.006 | 0.937 | 28 | 15 | χ2=0.201 | 0.654 | 24 | 19 | χ2=1.437 | 0.231 | |
| 否 | 60 | 24 | 58 | 26 | 56 | 28 | |||||||
| 肿瘤大小 | |||||||||||||
| T1 | 18 | 6 | Z=0.670 | 0.503 | 15 | 9 | Z=-0.571 | 0.568 | 16 | 8 | Z=0.590 | 0.556 | |
| T2 | 62 | 24 | 59 | 27 | 54 | 32 | |||||||
| T3 | 7 | 4 | 8 | 3 | 8 | 3 | |||||||
| T4 | 4 | 2 | 4 | 2 | 2 | 4 | |||||||
| 腋窝淋巴结转移 | |||||||||||||
| 阴性 | 16 | 5 | χ2=0.255 | 0.614 | 18 | 3 | χ2=3.728 | 0.054 | 18 | 3 | χ2=5.572 | 0.018 | |
| 阳性 | 75 | 31 | 68 | 38 | 62 | 44 | |||||||
| ER | |||||||||||||
| 阴性 | 21 | 12 | χ2=1.411 | 0.235 | 31 | 9 | χ2=2.557 | 0.110 | 34 | 8 | χ2=8.683 | 0.003 | |
| 阳性 | 70 | 24 | 55 | 32 | 46 | 39 | |||||||
| PR | |||||||||||||
| 阴性 | 29 | 18 | χ2=3.638 | 0.057 | 45 | 13 | χ2=4.757 | 0.029 | 49 | 14 | χ2=11.724 | 0.001 | |
| 阳性 | 62 | 18 | 41 | 28 | 31 | 33 | |||||||
| Ki-67 | |||||||||||||
| <14% | 22 | 9 | χ2=0.010 | 0.922 | 24 | 7 | χ2=1.766 | 0.184 | 19 | 12 | χ2=0.051 | 0.821 | |
| ≥14% | 69 | 27 | 62 | 34 | 61 | 35 | |||||||
| 分子分型 | |||||||||||||
| 非三阴性 | 71 | 27 | χ2=0.134 | 0.715 | 59 | 32 | χ2=1.219 | 0.270 | 50 | 38 | χ2=4.686 | 0.030 | |
| 三阴性 | 20 | 9 | 27 | 9 | 30 | 9 | |||||||
注:ER为雌激素受体;PR为孕激素受体;Ki-67为肿瘤增殖指数 |
表2 在不同阳性判定标准下新辅助化疗前后雌/孕激素受体表达一致组与差异组乳腺癌患者的肿瘤缓解率比较 |
| 标准及组别 | 例数 | 肿瘤缓解率(%) | 检验值 | P值 | |
|---|---|---|---|---|---|
| ≥1% | |||||
| 一致组 | 91 | 35.9±26.8a | t=2.190 | 0.032 | |
| 差异组 | 36 | 46.8±23.8a | |||
| >10% | |||||
| 一致组 | 86 | 37.3(21.4,53.6)b | |||
| 差异组 | 41 | 38.5(26.8,54.7)b | Z=0.446a | 0.656a | |
| >20% | |||||
| 一致组 | 80 | 39.1(22.7,55.1)b | |||
| 差异组 | 47 | 39.5(27.3,56.9)b | Z=0.548a | 0.584a | |
注:a正态分布数据,组间比较采用t检验;b偏态分布数据,组间比较采用秩和检验 |
表3 在不同阳性判定标准下新辅助化疗前后ER/PR表达变化的乳腺癌患者肿瘤缓解率比较( |
| 变化方式 | ≥1% | >10% | >20% | |||
|---|---|---|---|---|---|---|
| 例数 | 缓解率(%) | 例数 | 缓解率(%) | 例数 | 缓解率(%) | |
| ER阴转阳 | 7 | 36.4±27.7 | 7 | 30.9±32.4 | 6 | 28.5±34.9 |
| ER阳转阴 | 6 | 54.3±10.4 | 5 | 30.8±23.2 | 7 | 25.0±21.7 |
| PR阴转阳 | 9 | 58.1±22.9 | 11 | 53.2±23.3 | 13 | 48.0±25.7 |
| PR阳转阴 | 14 | 45.7±24.0 | 18 | 40.2±18.3 | 21 | 42.8±20.4 |
| F值 | 1.380 | 1.890 | 1.970 | |||
| P值 | 0.266 | 0.146 | 0.131 | |||
注:ER为雌激素受体;PR为孕激素受体 |
| [1] |
Spring L, Greenup R, Niemierko A, et al. Pathologic complete response after neoadjuvant chemotherapy and long-term outcomes among young women with breast cancer[J]. J Natl Compr Canc Netw,2017,15(10):1216-1223.
|
| [2] |
Masuda N, Lee SJ, Ohtani S, et al. Adjuvant capecitabine for breast cancer after preoperative chemotherapy[J]. N Engl J Med,2017,376(22):2147-2159.
|
| [3] |
Avci N, Deligonul A, Tolunay S, et al. Neoadjuvant chemotherapy-induced changes in immunohistochemical expression of estrogen receptor, progesterone receptor, HER2, and Ki-67 in patients with breast cancer[J]. J BUON,2015,20(1):45-49.
|
| [4] |
Cockburn A, Yan J, Rahardja D, et al. Modulatory effect of neoadjuvant chemotherapy on biomarkers expression; assessment by digital image analysis and relationship to residual cancer burden in patients with invasive breast cancer[J]. Hum Pathol,2014,45(2):249-258.
|
| [5] |
Allison KH, Hammond MEH, Dowsett M, et al. Estrogen and progesterone receptor testing in breast cancer: American Society of Clinical Oncology/College of American Pathologists Guideline Update[J]. Arch Pathol Lab Med, 2020,144(5):545-563.
|
| [6] |
Wolff AC, Hammond MEH, Allison KH, et al. Human epidermal growth factor receptor 2 testing in breast cancer: American Society of Clinical Oncology/College of American Pathologists Clinical Practice Guideline Focused Update[J]. J Clin Oncol, 2018,36(20):2105-2122.
|
| [7] |
Goldhirsch A, Wood WC, Coates AS, et al. Strategies for subtypes--dealing with the diversity of breast cancer: highlights of the St. Gallen International Expert Consensus on the Primary Therapy of Early Breast Cancer 2011[J]. Ann Oncol,2011,22(8):1736-1747.
|
| [8] |
Eisenhauer EA, Therasse P, Bogaerts J, et al. New response evaluation criteria in solid tumors: revised RECIST guideline (version 1.1) [J]. Eur J Cancer,2009,45(2):228-247.
|
| [9] |
Buzdar AU, Ibrahim NK, Francis D, et al. Significantly higher pathologic complete remission rate after neoadjuvant therapy with trastuzumab, paclitaxel, and epirubicin chemotherapy: results of a randomized trial in human epidermal growth factor receptor 2-positive operable breast cancer[J]. J Clin Oncol,2005,23 (16):3676-3685.
|
| [10] |
Shao Z, Pang D, Yang H, et al. Efficacy, safety, and tolerability of pertuzumab, trastuzumab, and docetaxel for patients with early or locally advanced ERBB2-positive breast cancer in Asia: the PEONY phase 3 randomized clinical trial[J]. JAMA Oncol,2020,6(3):e193692.
|
| [11] |
von Minckwitz G, Kümmel S, Vogel P, et al. Neoadjuvant vinorelbine-capecitabine versus docetaxel-doxorubicin-cyclophosphamide in early nonresponsive breast cancer: phase Ⅲ randomized GeparTrio trial[J]. J Natl Cancer Inst,2008,100(8):542-551.
|
| [12] |
杨文涛,步宏. 乳腺癌雌、孕激素受体免疫组织化学检测指南[J]. 中华病理学杂志,2015,44(4):237-239.
|
| [13] |
中国抗癌协会乳腺癌专业委员会.中国抗癌协会乳腺癌诊治指南与规范(2019年版)[J]. 中国癌症杂志,2019,29(8):609-680.
|
| [14] |
Gahlaut R, Bennett A, Fatayer H, et al. Effect of neoadjuvant chemotherapy on breast cancer phenotype, ER/PR and HER2 expression-implications for the practising oncologist[J]. Eur J Cancer,2016,60:40-48.
|
| [15] |
Yang L, Zhong X, Pu T, et al. Clinical significance and prognostic value of receptor conversion in hormone receptor positive breast cancers after neoadjuvant chemotherapy[J]. World J Surg Oncol,2018,16(1):51.
|
/
| 〈 |
|
〉 |